Die Bedeutung der Proteine ist schon in ihrem Namen enthalten, welche sich vom griech. Wort „proteos“ ableitet = erstrangig. Sie machen 50% des Trockengewichts der meisten Zellen aus und dienen als Werkzeuge für fast alle Aktivitäten des Organismus. Enzyme spielen eine zentrale Rolle.
Einfluss des Bindungspartner auf die Enzymaktivität
Wenn außer dem eigentlichen Substrat andere Stoffe an das Enzym binden wird die Enzymaktivität beeinträchtigt bzw. gehemmt. Konkurrieren 2 chemisch ähnliche Stoffe um das Bindungszentrum eines Enzyms beeinflusst dies die Enzymaktivität ist der chemisch ähnlicher Stoff ein Hemmstoff.
- Bindet am aktiven Zentrum, kann jedoch nicht umsetzt werden = Kompetitive Hemmung
- Wirkungsgrad ist abhängig von der Hemmstoffkonzentration
Bestimmte Enzyme besitzen nicht nur eine Bindungstelle für das Substrat, sondern eine weitere Bindungsstelle für ein anderes Molekül welches als Hemmstoff binden kann. Die Bindung bewirkt eine Konformationsänderung des Enzyms:
- Das Enzym ist ohne Bindung an der 2ten Bindungstelle aktiv –> Hemmstoff versetzt das Enzym in seine inaktive Form
- Das Enzym ist ohne Bindung an der 2ten Bindungsstelle inaktiv –> Aktivator versetzt das Enzym ist seine aktive Form
- = allosterische Hemmung
- Dient der Regulation vieler Stoffwechselprozesse
Kompetitive Hemmung
Hemmstoff bindet in das aktive Zentrum und blockiert es für Substrate –> Enzym vergiftet
Allosterische Hemmung
Inhibitor bindet an das Enzym und schließt es . –> Kein Zugang zu aktiven Zentrum für Substrate
Hemmung durch Schwermetalle
Bsp. Quecksilver, Blei, Kupfer
- Bewirken bei Enzymen Veränderung, die nicht rückgängig zu machen sind
- = irrevesibel
- sie zerstören die Disulfidbrücken und gehen mit Schwefel eine äußerst stabile Verbindung ein.
Temperatur und Milieu Abhängigkeit
Enzyme sind Biokatalysatoren. Jedes Enzym hat ein unterschiedliches optimum (ph; temp)
- PH: Sonst lösen Bindungen im Enzym auf –> Tertiär Struktur verändert sich (denaturierung)
- TEMP: Teilchen Bewegen sich schneller, Substrat und Enzym treffen wahrscheinlicher aufeinander; wird es aber zu heiß, lösen sich die Bindungen und und die Tertiärstruktur verändert sich (denaturierung)
Regulatoren
Negative Regulatoren
Verhindern, dass der Inhibitor aus der allosterischen Bindungstelle gelangen kann und erhalten so die inaktive Form –> Stabilisieren die negative Form
Positive Regulatoren
Verhindern das Andocken von Inhibitoren und sichern das Andocken des Substrats –> Sichern / stabilisieren die aktive Form
Entropieprinzip
Hohe Entropie bedeutet, dass sich das System in einem Zustand hoher Unordnung, und somit hoher Wahrscheinlichkeit eines Zusammenstoßes befindet
Endergonisch
Ein Prozess, bei dem die Entropie abnimmt. Nur unter ständiger Energiezufuhr möglich
Exergonisch
Prozess, bei dem die Entropie zunimmt
NAD und Coenzyme
NAD kann H-Atome übertragen, dabei wird aus NAD –> NADH. Nach der Reaktion mit Sauerstoff zu Wasser regeneriert sich das NAD. Vitamine werden als Coenzyme verwendet.
Energie und energetische Kopplung
Zellen und Energie
Für die vielen Stoffwechselvorgänge benötigt die Zelle Energie. Energie kann bei allen Prozessen weder erzeugt werden noch verloren gehen, da die Gesammtenergie im Isolierten System immer gleich bleibt (=Energieerhaltungssatz). Energieformen können sich zu anderen Umwandeln.
- Dynamisches Gleichgewicht: Die Energie innerhalb der Zelle ist immer gleich, sie wird verbraucht und anschließend von außen nachgeliefert.
- Statisches Gleichgewicht: Wird von außen keine Energie mehr nachgeliefert, kommt es zum Zelltod
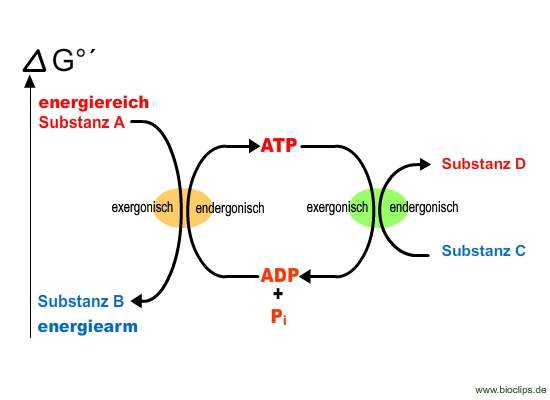
Energetische Kopplung
Energetische Kopplung bezieht sich im Allgemeinen auf das Zusammenspiel von verschiedenen Systemen, wobei Energie von einem System an ein anderes übertragen wird. Energetische Kopplung kann beispielsweise auf die Wechselwirkungen zwischen verschiedenen Organismen oder auf die Prozesse innerhalb einzelner Zellen bezogen werden.
- Spontan laufen Reaktionen ab, die zu einer Abnahme der Energie führen, das sind in der Regel Exotherme Reaktionen
- Das System strebt nach einem Energieminimum, da energiearme Zustände immer stabile Zustände sind.
Endotherme Vorgänge sind nur durch energetische Kopplung möglich: Ein Exothermer Prozess ermöglicht einen gleichzeitig stattfindenen endothermen Prozess


Bisher keine Kommentare